一塩化ヨウ素(いちえんかようそ、英iodine monochloride)は塩素とヨウ素が1対1で結合した無機化合物で、化学式IClで表される。赤褐色で、安定したα型と不安定なβ型があるが融点はいずれも常温に近い。ヨウ素と塩素の電気陰性度の違いから、I の供給源として作用する。一塩化ヨウ素は、ヨウ素と塩素の1:1の単純なモル比で構成される。
ヨウ素の結晶に塩素ガスを通すと一塩化ヨウ素の茶色の蒸気が生じ、冷却により一塩化ヨウ素の液体を得る。 塩素を過剰に供給することにより、可逆的に三塩化ヨウ素になる。
性質
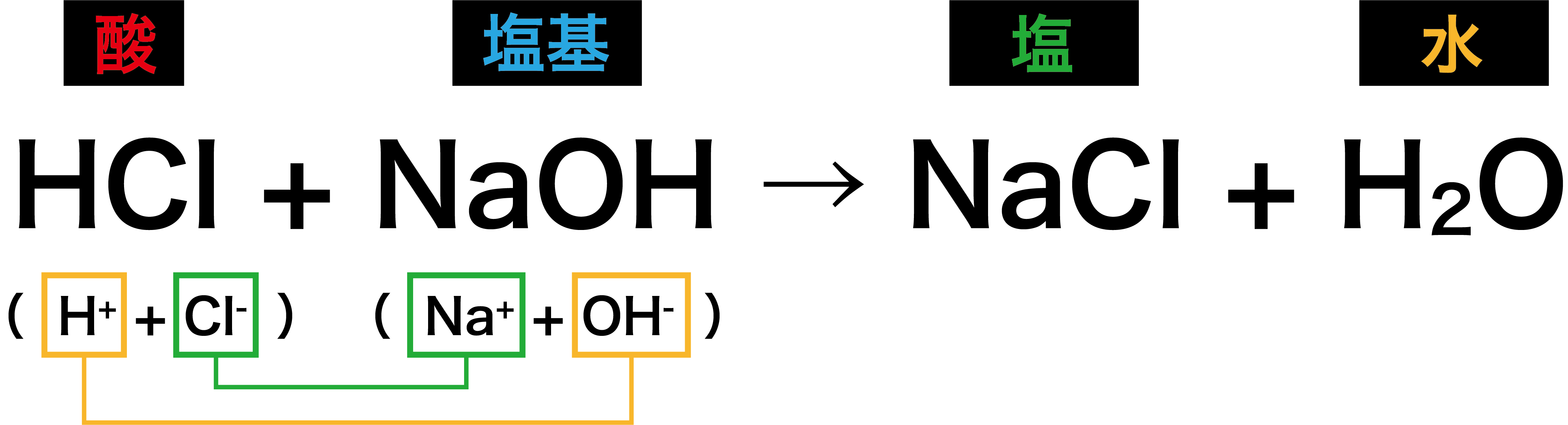
一塩化ヨウ素はα型とβ型の2つの同質異像を持つ。α型は黒色の針状結晶で、赤色の光を透過する。融点は27.2℃。β型は黒色の板状結晶で、赤茶色の光を透過する。融点は13.9℃。β型は―10℃から 5℃の間で液体から固体になるときに生じ、―10℃と0℃の間でのみ安定して存在する。カリウム・スズ・アルミニウム・水銀・銅・砒素・赤リン・テルルなどとは激しく反応するが、ナトリウム・マグネシウム・ニッケル・硫黄などとは穏やかに反応する。金属との反応では、塩化物およびヨウ化物を生じる。水に溶解して加水分解し、次亜ヨウ素酸と塩酸を生じる。
多くの有機溶媒に溶けるが、四塩化炭素、二硫化炭素、クロロホルム、ベンゼンなど無極性の溶媒では褐色、メタノール、エーテル、アセトン、ピリジン、酢酸など有極性の溶媒では黄色を呈する。
用途
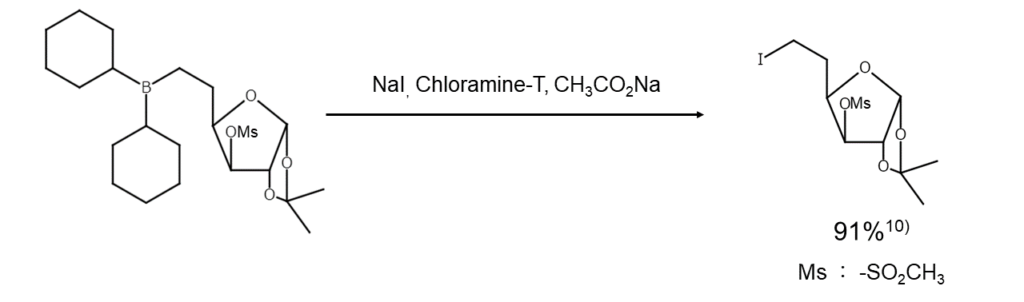
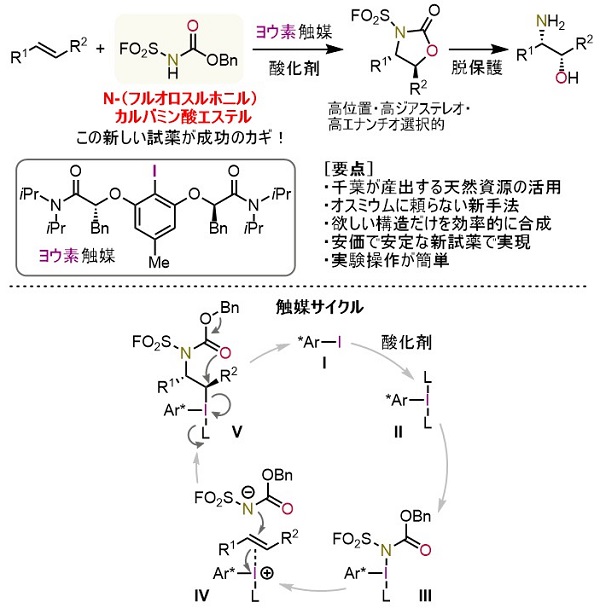
ウィイス法による油脂のヨウ素価測定に用いられる。芳香族ヨウ素化合物の製造においてはヨウ素供給源として働き、炭素とケイ素の結合を切断するなど、有機合成で重要な役割を果たす。 また、アルケンの二重結合に塩素・ヨウ素を含むアルカンを付与する。
この反応は、アジ化ナトリウムの存在下で行われる。
脚注